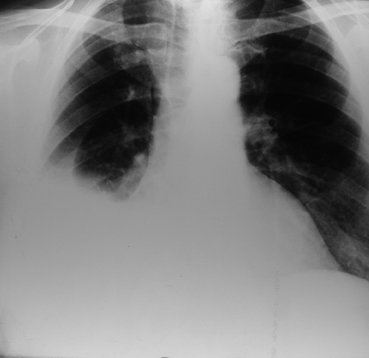
Varón de 57 años, con diagnóstico de hepatopatía crónica en fase cirrótica
INTRODUCCIÓN
Todo derrame pleural con características de trasudado que aparece en un paciente cirrótico en ausencia de una enfermedad cardiaca o pulmonar de base se denomina hidrotórax del cirrótico. Su formación no depende de la etiología de la hepatopatía crónica sino del desarrollo de hipertensión portal y debido a esto, puede presentarse en otras condiciones clínicas que se asocien a un aumento de la presión portal sin cirrosis. Habitualmente se forma en el hemitórax derecho y puede asociarse o no a ascitis. Todo paciente con este diagnóstico debe ser evaluado para transplante hepático ya que suele asociarse a un estadio terminal de la enfermedad hepática. El manejo se basa en el uso de diuréticos y otros tratamientos médicos e intervencionistas.
CASO CLÍNICO
Un paciente varón de 57 años, con diagnóstico de hepatopatía crónica en fase cirrótica, de etiología alcohólica asociada a virus C, con el desarrollo de várices esofágicas, consulta por disnea a moderados esfuerzos. Se encuentra en tratamiento con ciprofloxacina para profilaxis de PBE, propranolol y dieta hiposódica que cumple parcialmente.
Al examen físico presenta frecuencia respiratoria normal, escleras subictéricas, nevus estelares aislados en cara y tronco, hipoventilación marcada en campo pulmonar derecho con matidez a la percusión, escasa matidez desplazable en hemiabdomen inferior, edemas en miembros inferiores con Godet +, sin encefalopatía.
Se realiza RX de tórax que evidencia derrame pleural derecho.
En el laboratorio presenta pO2 63 mmHg, saturación 92%, Hto 26%, GB 3420/mm3, plaquetas 55000/mm3, glicemia, uremia, ionograma normales, ASAT 124 UI/L, ALAT 64 UI/L, FAL y GGT normales, bilirrubinemia total 3.4 mg/dl, proteínas totales 6.6 gr/dl, albuminemia 2.8 gr/dl, tasa de protrombina 42%, LDH 529 UI/L.
No se pudo obtener muestra de líquido ascítico por escasa cantidad del mismo.
Se realiza toracocentesis de 400 ml. En el líquido pleural presenta pH 7.44, 15 elementos/mm3, glucosa 1, proteínas totales 4, colesterol 4 mg/dl, triglicéridos 48 mg/dl, LDH 74.
Se interpreta como HIDROTÓRAX DEL CIRRÓTICO comenzado tratamiento con espironolactona, fursemida y dieta hiposódica estricta con buena respuesta.
DISCUSIÓN
El HIDROTÓRAX HEPÁTICO es todo aquel derrame pleural, generalmente mayor a 500 ml, que aparece en un paciente con cirrosis e hipertensión portal en ausencia de una enfermedad cardiopulmonar.
Es una complicación infrecuente de la cirrosis hepática. Se observa sólo en el 5-12% de los pacientes cirróticos y constituye una manifestación de una enfermedad descompensada similar a la presencia de ascitis, encefalopatía hepática o hemorragia variceal.
La hipertensión portal es la base fisiopatogénica de su origen. Por lo tanto, puede formarse en ausencia de cirrosis en otras enfermedades que cursan con presión portal elevada.
El líquido se origina en la cavidad peritoneal y no en la pleura. Es líquido ascítico que se moviliza desde el abdomen hacia la pleura a través de defectos en el diafragma. Mediante el examen microscópico se demostró que estos defectos se forman por discontinuidad de las bandas colágenas que constituyen la porción tendinosa del diafragma. El aumento en la presión intraabdominal por la acumulación de ascitis, la tos o hacer fuerza produciría la herniación del peritoneo hacia la cavidad pleural a través de estas brechas produciendo “blebs” pleuroperitoneales. Estos blebs que suelen medir menos de 1 cm podrían romperse y producir una comunicación libre entre ambas cavidades. La migración de líquido ascítico se daría en forma unidireccional hacia el espacio pleural debido a que la presión dentro de la pleura es negativa en relación a la presión intraabdominal. Cuando la tasa de flujo que ingresa a la cavidad pleural excede la capacidad que tiene la pleura para reabsorber el líquido, éste se acumula y se produce el hidrotórax hepático.
Se desconoce el motivo por el cual es más frecuente del lado derecho pero estaría relacionado con el desarrollo embriológico ya que el hemidiafragma izquierdo es más grueso y muscular.
El domo hepático puede oponerse a los defectos en el hemidiafragma derecho permitiendo la fuga directa de líquido hacia la pleura sin acumularse en forma importante en la cavidad peritoneal. Por eso, en algunos casos, puede no acompañarse de ascitis o ser mínima.
El hidrotórax hepático se debe sospechar en todo paciente cirrótico con disnea, tos seca o dolor pleurítico. Incluso se puede manifestar con fatiga por hipoxemia. A diferencia de la ascitis, pequeñas cantidades de líquido pleural suelen ser mal toleradas y la severidad de los síntomas depende del volumen de líquido acumulado. En pocos casos se presenta con insuficiencia respiratoria o hipotensión por hidrotórax agudo a tensión.
En el 65-87% de los casos es derecho, con menor frecuencia puede ser izquierdo (13%), y rara vez, bilateral (2%).
En la mayoría de los casos es de pequeña o moderada cantidad. Sin embargo, en aproximadamente 6% de los pacientes puede ser de gran volumen ocupando más de la mitad del hemitórax. A pesar de esto, los derrames que se acumulan lentamente en pacientes debilitados por una enfermedad hepática crónica suelen ser relativamente asintomáticos aun cuando el volumen es grande.
Para el diagnóstico se deben analizar ambos líquidos, tanto el ascítico como el pleural. El líquido pleural es típicamente un trasudado. El recuento de células es menor a 500/mm3, con predominio de mononucleares (polimorfonucleares <250/mm3), las proteínas totales son menores a 2.5 gr/dl, la lactato dehidrogenasa (LDH) es baja y el gradiente sérico-pleural de albúmina es mayor a 1,1 g/dl, similar al GASA que resulta de la hipertensión portal. Otros parámetros a tener en cuenta son: cociente proteínas totales en líquido pleural/suero <0.5, cociente LDH en líquido pleural/suero >0.6, pH >7.4 y concentración de glucosa similar al plasma. Los niveles de proteínas, albúmina y lípidos en el líquido pleural tienden a ser levemente superiores a los del líquido ascítico. Esta diferencia podría atribuirse a que la pleura es más eficaz para absorber agua.
En la hipertensión portal existe aumento del flujo linfático. La ruptura de algún vaso linfático puede dar lugar a un quilotórax hepático. Debido a que la linfa se diluye en el líquido ascítico, el nivel de triglicéridos y el recuento de linfocitos suele ser menor que en otras formas de quilotórax y el líquido conserva las características de trasudado.
Habitualmente se acompaña de ascitis pero en algunos casos ésta no es clínicamente evidente. Cuando existan dudas sobre el origen del hidrotórax (localización izquierda o sin ascitis) se puede recurrir a estudios de medicina nuclear. Mediante la inyección intraperitoneal de un trazador (99mTc-sulfuro coloidal o 99mTc-albúmina humana) se puede demostrar el rápido pasaje del radioisótopo a través del diafragma y su acumulación en la cavidad pleural con una sensibilidad y especificidad de 71% y 100%, respectivamente. Sin embargo, es un estudio poco utilizado en la práctica clínica. La resonancia magnética o la videotoracoscopía podrían detectar los defectos diafragmáticos subyacentes.
En algunos pacientes puede ser necesario realizar un ecocardiograma para descartar alguna cardiopatía o una tomografía de tórax si se sospecha una enfermedad intratoráxica oculta. En un estudio reciente se demostró que el 18% de los pacientes cirróticos con derrame pleural tenían otra patología no hepática como causante del mismo. Por eso, algunos autores postulan que en todos los casos se debería realizar una tomografía de tórax para descartar patología pulmonar, mediastinal o pleural. Si se sospecha una neoplasia y la citología del líquido pleural es no concluyente se podría realizar una toracoscopía con toma de biopsia.
Una complicación del hidrotórax del cirrótico es el EMPIEMA BACTERIANO ESPONTÁNEO o PLEURITIS BACTERIANA ESPONTÁNEA. Un 13% de los pacientes con hidrotórax tienen un empiema al momento del ingreso. Es una complicación severa con elevada mortalidad (20%). Se debe sospechar ante un paciente con hidrotórax hepático y fiebre, dolor pleurítico, encefalopatía y/o deterioro clínico sin causa evidente. Los criterios diagnósticos son un recuento de polimorfonucleares en el líquido pleural >500/mm3 o >250/mm3 con cultivo positivo en ausencia de neumonía u otro foco infeccioso por contigüidad. Es una condición análoga a la peritonitis bacteriana espontánea (PBE) y los gérmenes responsables son similares (Escherichia coli, Streptococcus spp., Enterococcus, Klebsiella, Aeromonas). La patogénesis permanece desconocida. En algunos individuos, la infección pleural se produciría como consecuencia del pasaje de líquido peritoneal infectado (asociación con PBE 50%). En otros, el cultivo de líquido ascítico es negativo y sería consecuencia de una bacteriemia. Incluso no siempre se acompaña de ascitis. Puede conservar las características de trasudado y rara vez es purulento. Los factores de riesgo para un empiema espontáneo son el score de Child-Pugh C y niveles bajos de proteínas totales y C3 en el líquido pleural. El tratamiento es similar al de la PBE (cefalosporina de 3º generación durante 7-10 días).
TRATAMIENTO
El hidrotórax hepático es una complicación de una hepatopatía crónica en fase terminal. Todos los pacientes deben ser evaluados para transplante hepático.
No nos debemos olvidar que es líquido ascítico que ha entrado a la cavidad pleural. Por lo tanto, el manejo médico inicial es idéntico al de la ascitis. La primera línea de tratamiento es la restricción de sodio y los diuréticos. Existen reportes aislados del uso de octreotide, terlipresina y ncpap (nasal continuous positive airway pressure) con buena respuesta. Sin embargo, estos resultados deben ser confirmados en estudios con series de pacientes.
En aquellos pacientes con disnea importante y dificultad respiratoria se puede realizar una toracocentesis evacuadora que se repetirá en los casos recurrentes o refractarios. El principal riesgo de este procedimiento es el neumotórax que aumenta con las sucesivas punciones. Nunca se debe drenar más de 2 litros de líquido pleural debido al riesgo de hipotensión y edema pulmonar por reexpansión. Cuando se requiera más de una toracocentesis terapéutica cada 2 semanas en pacientes en tratamiento estricto con restricción de sodio y diuréticos a dosis óptima, se deberán considerar otras opciones terapéuticas.
En la actualidad no se aconseja colocar un tubo de drenaje pleural. Se ha intentado la pleurodesis mediante la instilación de tetraciclina o talco a través del mismo con resultados decepcionantes. La rápida reacumulación de líquido impide la adhesión de ambas hojas pleurales y las complicaciones son muy frecuentes (fiebre, empiema, dolor torácico, neumonía, reexpansión incompleta, infección de la herida).
En la mayoría de los pacientes con un hidrotórax hepático resistente al tratamiento médico y/o toracocentesis terapéuticas a repetición, el procedimiento de elección es la colocación de un TIPS (transjugular intrahepatic portosystemic shunt). Se han reportado tasas de éxito de 58% que aumentan a 82-91% si entre los criterios de respuesta se considera una disminución en el volumen del hidrotórax o un menor requerimiento de toracocentesis. Entre las complicaciones más frecuentes se encuentran la obstrucción del stent, encefalopatía hepática y agravamiento de una hipertensión pulmonar preexistente.
La toracoscopía con reparación del defecto diafragmático con o sin pleurodesis es una alternativa válida en aquellos pacientes no candidatos al TIPS o en espera de un transplante hepático. Este procedimiento es más eficaz si se detecta la anormalidad anatómica. Sin embargo, la toracoscopía con pleurodesis sola brinda buenos resultados.
Finalmente, si el tratamiento médico falla, se debe recurrir al transplante hepático siendo el TIPS o la toracoscopía medidas temporales utilizadas como puente hasta la aparición de un órgano compatible.
BIBLIOGRAFIA
- Cárdenas, V. Arroyo. Management of ascites and hepatic hydrothorax. Best Pract Res Clin Gastroenterol 2007;21(1):55-75
- Garrido Serrano, J. M. Pascasio Acevedo, J. L. Márquez Galán. Tratamiento con octreótido en el hidrotórax hepático. Rev Esp Enferm Dig 2006;98(8):625-634
- G. Therapondos, F. Wong. Miscellaneous indications for transjugular intrahepatic portosystemic stent-shunt. Eur J Gastroent Hepatol 2006;18:1161–1166
- R. Cerfolio, A. Bryant. Efficacy of Video-Assisted Thoracoscopic Surgery With Talc Pleurodesis for Porous Diaphragm Syndrome in Patients With Refractory Hepatic Hydrothorax. Ann Thorac Surg 2006;82:457–459
- T-W Huang, Y-L Cheng, H Chang, S-C Lee, J-C Chen. Hepatobiliary and pancreatic: Hepatic hydrothorax. J Gastroent Hepatol 2007;22:956
- G. Kalambokis, E. Tsianos. Treatment of hepatic hydrothorax with vasoconstrictor drugs. Scand J Gastroenterol 2007;42:534-535
- K. Dohmen, H. Tanaka, M. Haruno, Y. Niho. Hepatic hydrothorax occurring rapidly after manual abdominal compression. World J Gastroenterol 2007;14; 13(46):6284-6285
- G. Kinasewitz, J. I. Keddissi. Hepatic hydrothorax. Curr Opin Pulm Med 2003;9:261–265
- Roussos, N. Philippou, G. Mantzaris, K. Gourgouliannis. Hepatic hydrothorax: Pathophysiology diagnosis and management. J Gastroenterol Hepatol 2007;22:1388–1393